2.6. Nervensystem#
- Liquor cerebrospinalis
Produktion im Plexus choroideus, Absorption an Arachnoidalvilli der Sinus durae matris durch hydrostatischen Druckgradienten.
Zusammensetzung: weniger Kalium, Bikarbonat und Glucose als im Plasma, Protein nur in Spuren (0,2 g / l während Plasma 75 g / l).
- Einteilung
Somatisches NS (willkürlich) und unwillkürliches NS (Parasympathikus + Sympathikus)
- Peripherer Nerv
Axon-Myelinscheide-Endoneurium-Perineurium-Faszikel-Epineurium
- Neuron
Soma mit Zellkern-Axon-Dendriten
- Aktionspotential
Das Ruhemembranpotential (Kaliumdiffusionspotential bei geschlossenen Na-Kanälen) beträgt minus 80mV. Na/K-Pumpe bringt Natrium entgegen dem Konzentrationsgradienten aus der Zelle und Kalium in die Zelle, bei -50mv Schwellenwert kommt es zum Na-Einstrom = Depolarisation mit Aktionspotential (Alles-oder-nichts-Regel)
Danach passiver Kaliumausstrom mit Repolarisation = refraktär (nicht erregbar). Das Ruhemembranpotential ist weniger negativ bei: Hyperkaliämie, inaktivierten Na/K-Pumpen.
- Synapsen
Elektrisch (gap junctions) und chemisch (Transmitter mit postsynaptischem Rezeptor und Öffnung von Membrankanälen; Inaktivierung des Transmitters durch Re-uptake oder Hydrolyse). Ist das postsynaptische Potential positiv = exzitatorische Synapse, und wenn das PSP negativ ist, ist es eine inhibitorische Synapse:
Erregend: Acetylcholin, Glutaminsäure
Hemmend: GABA, Glycin, Serotonin, Dopamin
- Ligandengesteuerte Rezeptoren
Direkte Wirkung auf Ionenkanal, wirken schnell, z.B. GABA
Indirekte Wirkung über G-Protein und second messenger cAMP, z.B. Katecholamine
2.6.1. Das vegetative Nervensystem#
= komplexes Zusammenspiel von Parasympathikus und Sympathikus zur Regelung der Organfunktion, Kontrolle des inneren Milieus und Anpassung des Körpers an äußere Verhältnisse.
Ursprung ist im ZNS:
Hypothalamus: Wasserhaushalt, Körpertemperatur, Nahrungsaufnahme
Hirnstamm: Atmung, Husten, Kreislauf, Erbrechen, Schlucken
Afferenzen:
Aus der Peripherie z.B. Vagus
Innere Rezeptoren: CO2, O2, pH-Rezeptoren
Nervenfasern sind präganglionär B-Fasern und postganglionär C-Fasern.
- Neurotransmitter
Sympathikus: ganglionär Acetylcholin, postganglionär Noradrenalin
Parasympathikus: ganglionär Acetylcholin, postganglionär Acetylcholin.
- Lage der Ganglien des Sympathikus
Zellkörper des 1 Neuron Th1/2 im RM, Umschaltung im Grenzstrang des 2 Neurons führt zum Zielorgan.
- Lage der Ganglien des Parasympathikus
Ursprung des 1 Neuron in den Kerngebieten der Hirnnerven III, VII, IX, X (besonders Vagus) und S2-5. Die Umschaltung auf das 2 Neuron findet erst im Zielorgan statt.
- Acetylcholin
wird aus Cholin und Acetyl-CoA synthetisiert und durch Cholinesterase gespalten.
Cholinesterasen#
Es gibt drei verschiedene Cholinesterasen:
Ortsständige spezifische CHE (f. Acetylcholin)
Plasma-CHE: spaltet Succinylcholin, Mivacron, Ester-LA (Procain, Cocain)
Unspezifische CHE: Abbau von Ultiva, Esmolol
Acetylcholinrezeptoren:#
An der motorischen Endplatte: nikotinerger Rezeptor N2
Präganglionär ParaS + zwischen 1 und 2 Neuron im Sympathikus: Nikotinerger Rezeptor: N1
Postganglionär ParaS: muskarinerger Rezeptor
Indirekte Hemmung am Acetylcholin-Rezeptor durch Hemmung der Cholinesterase:#
Neostigmin (Prostigmin™), nicht ZNS gängig, Antagonisierung der Muskelrelaxierung, verdrängt Muskelrelaxans vom Rezeptor.
Physostigmin (Anticholium™): ZNS gängig bei ZAS (zentrales anticholinerges Syndrom)
Pyridostigmin (Mestinon™): Myasthenia gravis Therapie
- NW der Antagonisierung
Bradykardie, Salivation, Bronchospasmus, daher Kombination mit Parasympatholytika (Atropin, Robinul), welche jedoch Tachykardie, Hypertonie, Sekretions-Stop, Mydriasis, Fieber bei Kindern durch verminderte Schweißproduktion, Agitation, und Angst bewirken können.
2.6.2. zentrales Anticholinerges Syndrom:#
Es gibt eine delirante oder somnolente Form.
- Bei beiden findet man klinisch
weite Pupillen, Schluckstörung, Mundtrockenheit, Tachykardie, ev. Extrasystolen, Harnverhalt.
- Auslöser
sind Atropin, Antihistaminika, Benzodiazepine, Ketamin, volatile Anästhetika,…
- Therapie
Physostigmin titriert. (Anticholium™)
2.6.3. Sympathomimetika#
Wirken über….
α1-Rezeptoren: bewirken Vasokonstriktion, hemmen Sekretion, Mydriasis, Tonussteigerung bei Uterus und Blase, hemmen Insulinfreisetzung; kommen überall vor, in Herz und Gehirn vermindertes Vorkommen.
α2-Rezeptoren: haben vor allem eine präsynaptische Funktion. Sie wirken im ZNS sedierend, KRL: Bradykardie, Hypotonie, hemmen NA-Ausschüttung über negative Feedback Schleifen.
β1-Rezeptoren: Im Herz positiv inotrop, chronotrop, dromotrop, siehe Betablocker!
β2-Rezeptoren: vor allem postsynaptisch, überall nur im Herzen wenig; Vasodilatation, Brochodilatation, Tokolyse, steigern Insulinsekretion, steigern Gluconeogenese und Glycogenolyse, steigern NA-Ausschüttung über positives Feedback.
β3-Rezeptoren: im Fettgewebe, Lipolyse
D1-Rezeptoren: postsynaptisch für Vasodilatation im Splanchnikusgebiet, Hirn- und Koronararterien, steigern Nierendurchblutung.
D2-Rezeptoren: präsynaptisch, NA-Ausschüttung im ZNS, antiemetisch
- Stress
= Adrenalin und NA-Ausschüttung durch Sympathikusaktivierung von β und α-Rezeptoren mit erhöhter HF, Kontraktilität, Bronchodilatation, Vasokonstriktion, erhöhter Koronarperfusion, Glykogenolyse und Lipolyse. Ziel ist Verbesserte Sauerstoff- und Substratversorgung von Herz, Muskel und Gehirn.
- Abbau von Noradrenalin und Adrenalin
Über COMT und MAO mit Vanillinmandelsäure als Endprodukt im Harn. (Phäochromozytomdiagnostik!)
- L-Adrenalin/Suprarenin
Dosisabhängige Wirkung:
< 2 µg / min β2-Stimulation mit Broncho- und Vasodilatation,
von 2–10 µg / min β1 und β2 Stimulation mit Zusätzlich positiv Inotropie, Chronotropie und Dromotropie (Patient wird tachykard und bekommt Herzrhythmusstörungen).
> 10 µg / min erfolgt vor allem eine α1-Stimulation mit Vasokonstriktion = CPR mit fixer Dosierung unabhängig vom KG!
- Noradrenalin/Arterenol
Bewirkt vor allem eine α1 und α2-Stimulation mit Vasokonstriktion ohne Herzfrequenzanstieg;
(Wirkt auch auf β1-Rez., aber durch Blutdruckanstieg → Barorezeptoren → eher Reflexbradykardie)
Dosierung 2-20 µg / min
Bei 0,1 mg / ml z.B.:
3,5 ml / h = 350 µg / h,
60 min = 5,8 µg / min,
bei 80 kg: 0,07 µg / kg / min = Gamma!
> 0,5 ist sehr hoch!
Was ist Gamma?
Als “Gamma” werden umgangssprachlich µg / kg / min bezeichnet
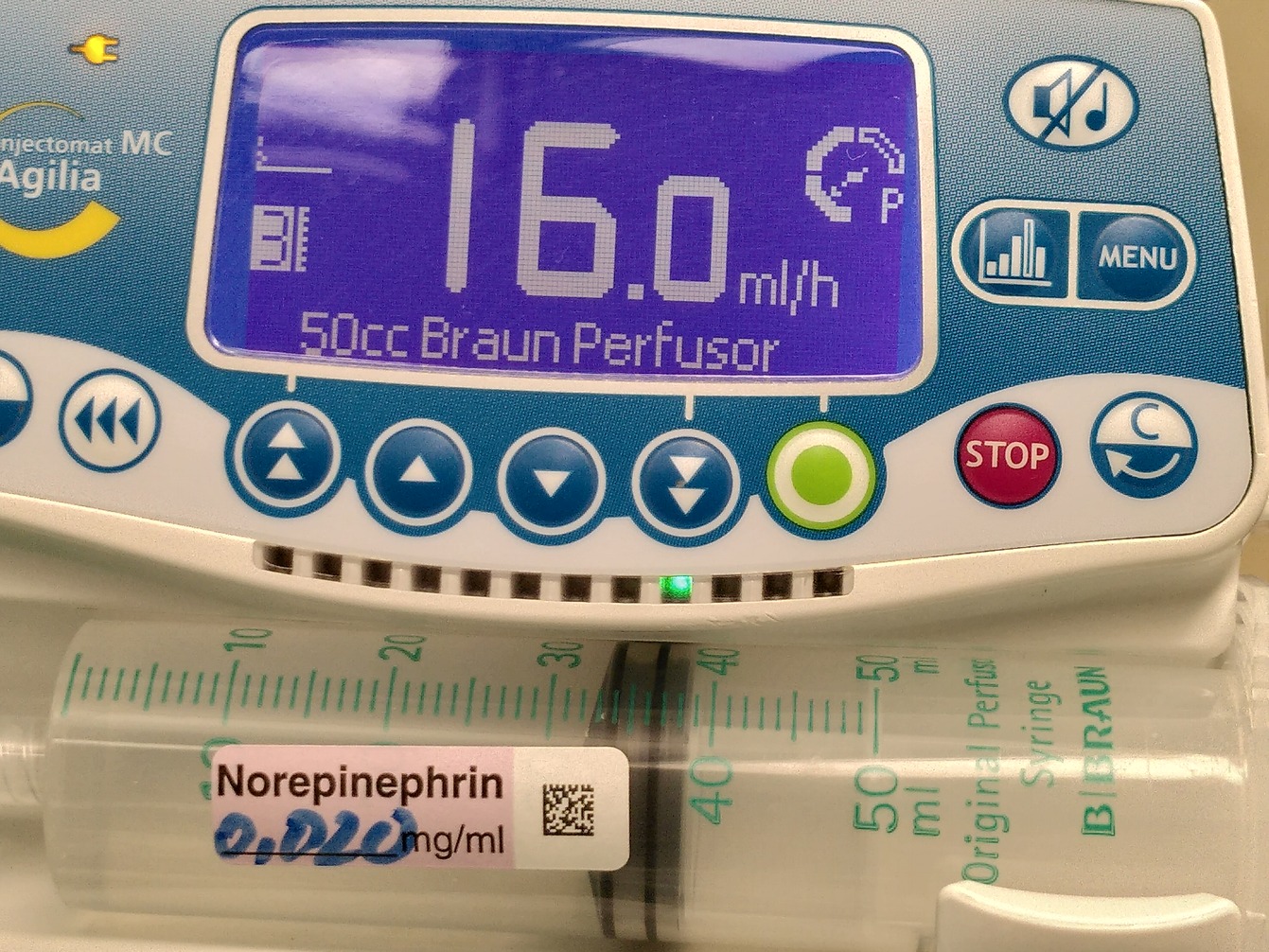 Noradrenalin
Noradrenalin
 Noradrenalin-Schenkel
Noradrenalin-Schenkel
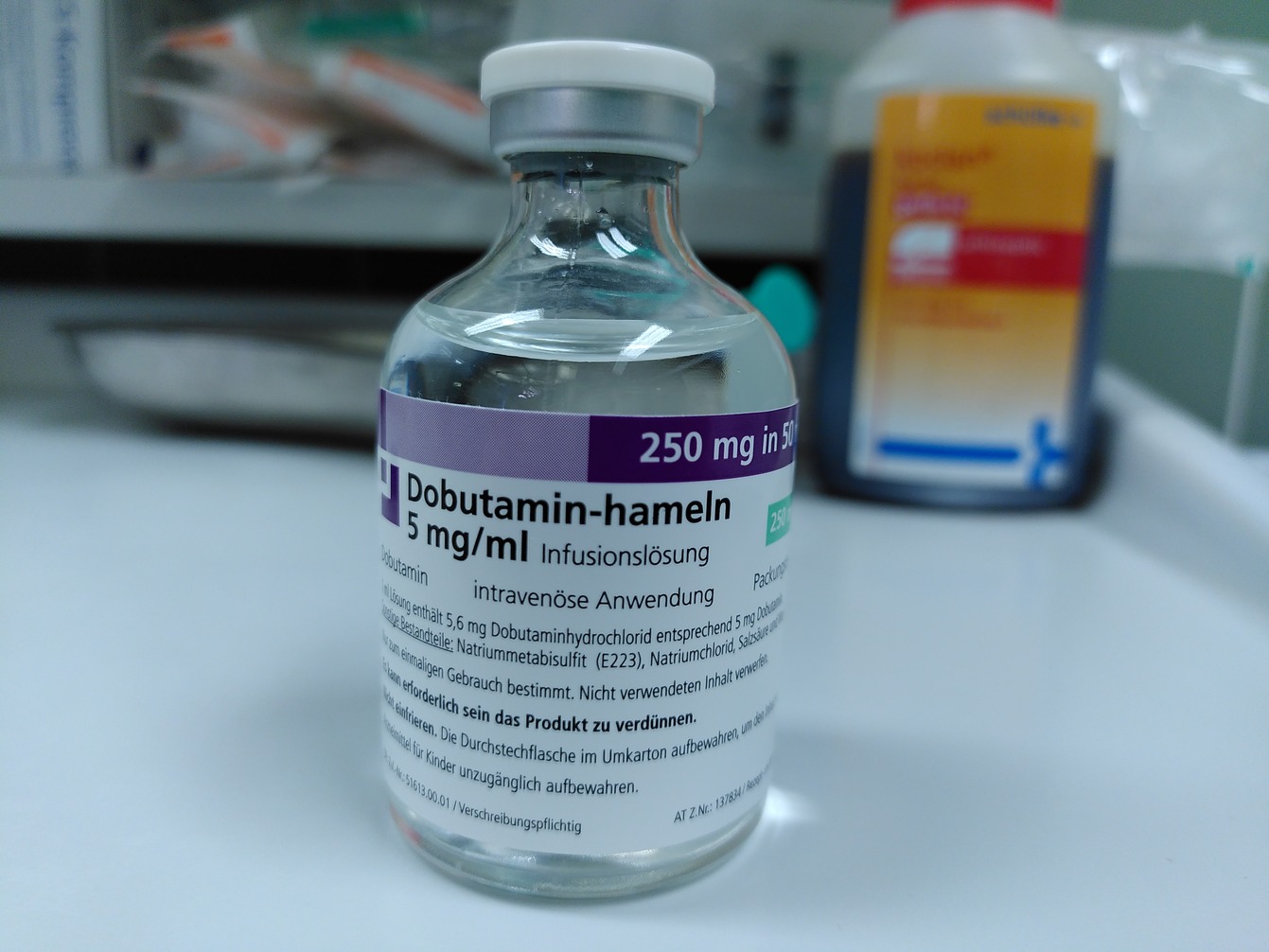 Dobutamin
Dobutamin
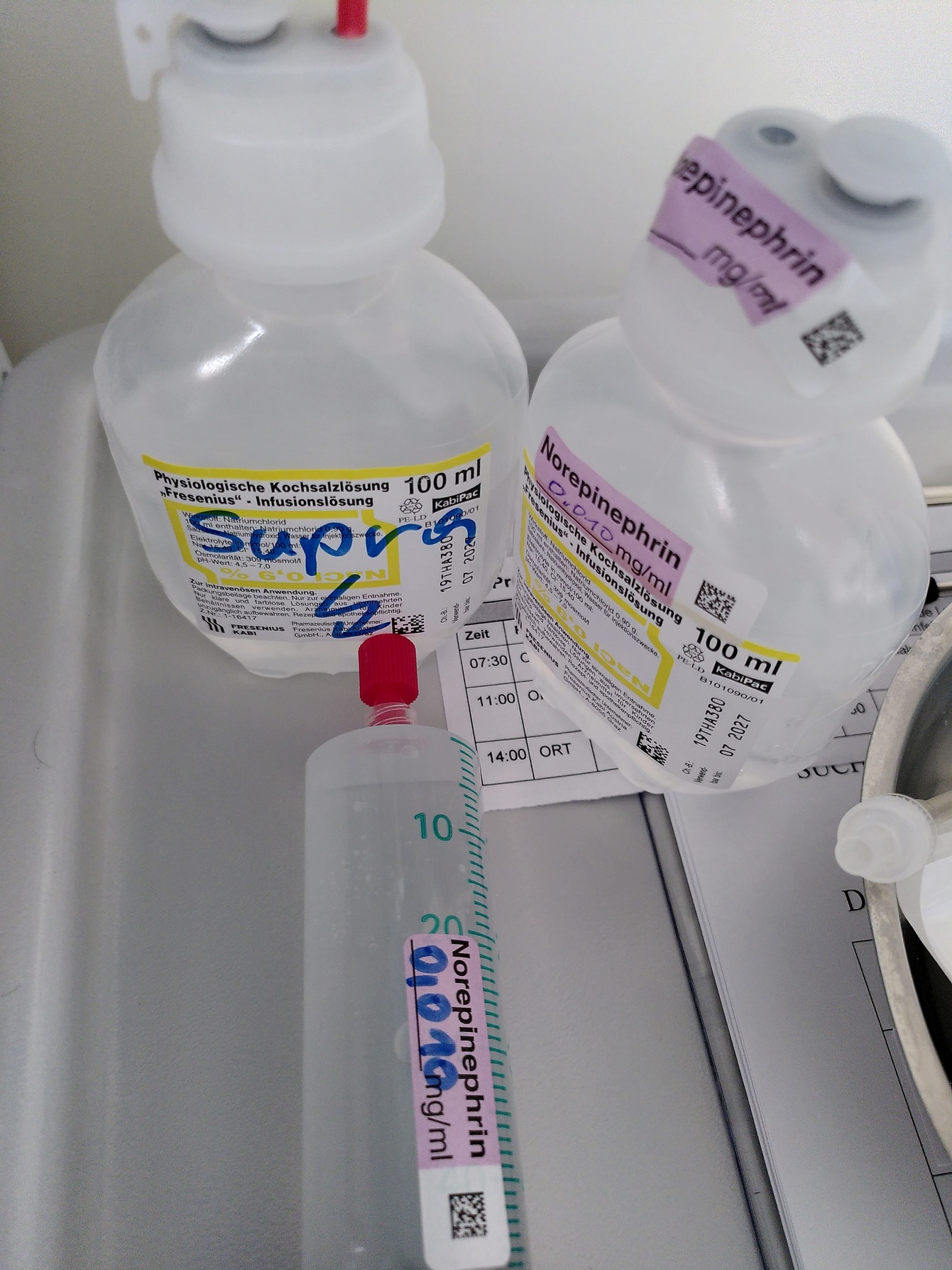 Adrenalin
Adrenalin
Fig. 4 Katecholamine#
- Dopamin
Dosisabhängige Wirkung:
< 2 µg / kg / min D1-Stimulation mit renaler Vasodilatation und gesteigerter Diurese;
2-10 µg / kg / min β1-Stimulation mit positiv inotrop, chronotrop, dromotrop mit gesteigertem kardialem VO₂;
> 10 µg / kg / min α1-Stimulation mit Vasokonstriktion.
- Dobutamin/Dobutrex
selektiver β1-Agonist mit verbesserter Inotropie ohne Blutdruckanstieg aber mit Herzfrequenzanstieg.
- Phenylephrin (Neosynephrin™)
synthetisches Nicht-Katecholamin, bewirkt eine α1-Stimulation mit Blutdruckanstieg und oft Reflexbradykardie.
- Ephedrin
α+β-Agonist, Blutdruck und Herzfrequenzanstieg.
- Praktische Anwendung
Hypotonie mit Bradykardie: Ephedrin (aber: ab 50 mg NA-Speicher leer, keine weitere Wirkung zu erwarten)
Hypotonie mit Tachykardie: NA, Phenylephrin
- Clonidin
α2-Agonist, lipophil, gute zentrale Hemmung der NA-Freisetzung, antihypertensiv, Entzugsdelir, Verlängert LA-Wirkung (Caudalblock), senkt Narkosebedarf, verbessert Kreislaufstabilisierung während AN durch Reduktion der zirkulierenden Katecholamine/Sympathikotonus.
NW: Bradykardie, Hypotonie, Polyurie, Obstipation.
- Dexmedetomidine (Dexdor™)
hochselektiver α2-Agonist; Wirkt sedativ-hypnotisch, mit Änderung des Schlafmusters wie im natürlichen Schlaf, unveränderter CO₂-Atemantrieb; Wirkt analgetisch im Locus caeruleus und RM, bei akuten, neuropathischen und Tumorschmerzen.
NW: Verlängert Refraktärzeit am AV-Knoten
Zugelassen zur Delirtherapie, off label use zur Sedoanalgesie bei kleinen Eingriffen.
2.6.4. Sympatholytika#
- α1-Blocker
Urapidil (Ebrantil™) senkt den Blutdruck, kardiale Entlastung bei Herzinsuffizienz.
- β1-selektive Blocker
bei SVT, VT, paroxysmalen Tachykardien, MCI, Hypertonie,… z.B. Brevibloc, Metoprolol (Beloc™, siehe Betablocker)